Ora nel mondo c'è un'enorme quantità di farmaci, provenienti da quasi tutte le malattie esistenti. La creazione di un nuovo farmaco non è solo un'attività a lungo termine, ma anche costosa. Dopo che il medicinale è stato creato, è necessario testare come agisce sul corpo umano, quanto sarà efficace. A tal fine, sono in corso studi clinici di cui parleremo nel nostro articolo.
Il concetto di ricerca clinica
Qualsiasi ricerca sui farmaci è semplicemente necessaria, come una delle fasi dello sviluppo di un nuovo farmaco o per espandere le indicazioni per l'uso di uno esistente. Inizialmente, dopo aver ricevuto la medicina, tutti gli studi sono condotti su materiale microbiologico e animali. Questo stadio è anche chiamato studi preclinici. Vengono effettuati per ottenere prove dell'efficacia dei farmaci.
Ma gli animali sono diversi dagli umani, quindi il modo in cui i topi sperimentali rispondono al farmaco non significa ottenere la stessa reazione nell'uomo.
Se definiamo quali sono gli studi clinici, allora possiamo dire che si tratta di un sistema che utilizza vari metodi per determinare la sicurezza e l'efficacia di un medicinale per una persona. Durante lo studio del farmaco, tutte le sfumature sono chiarite:
- Effetti farmacologici sul corpo.
- Tasso di aspirazione.
- La biodisponibilità del farmaco.
- Periodo di attesa.
- Caratteristiche del metabolismo.
- Interazione con altre medicine.
- Sicurezza per l'uomo.
- La manifestazione di effetti collaterali.
Gli studi di laboratorio iniziano con la decisione dello sponsor o del cliente, che sarà responsabile non solo dell'organizzazione, ma anche del controllo e del finanziamento di questa procedura. Molto spesso, una persona simile è la società farmaceutica che ha sviluppato questo farmaco.
Tutti i risultati degli studi clinici, i loro progressi dovrebbero essere descritti in dettaglio nel protocollo.
Statistiche di ricerca
Lo studio dei farmaci viene condotto in tutto il mondo, questo è un passaggio obbligatorio prima di registrare un farmaco e il suo rilascio di massa per uso medico. Quei fondi che non sono stati testati non possono essere registrati e immessi sul mercato dei farmaci.
Secondo una delle associazioni americane dei produttori di farmaci di 10 mila dei farmaci studiati, solo 250 raggiungono lo stadio degli studi preclinici, di conseguenza, gli studi clinici saranno condotti solo per circa 5 farmaci e 1 raggiungerà la produzione e la registrazione in serie. Questa è la statistica.
Obiettivi di ricerca di laboratorio
La ricerca su qualsiasi farmaco ha diversi obiettivi:
- Stabilire come questo farmaco è sicuro per l'uomo. Come il corpo lo tollererà. Per fare questo, trova volontari che accettano di partecipare allo studio.
- Durante lo studio, vengono selezionate le dosi e i regimi di trattamento ottimali per ottenere il massimo effetto.
- Stabilire il grado di sicurezza del farmaco e la sua efficacia per i pazienti con una certa diagnosi.
- Studiare effetti collaterali indesiderati.
- Valuta la possibilità di espandere il consumo di droga.
 Abbastanza spesso, gli studi clinici sono condotti simultaneamente per due o anche tre farmaci, in modo che la loro efficacia e sicurezza possano essere confrontate.
Abbastanza spesso, gli studi clinici sono condotti simultaneamente per due o anche tre farmaci, in modo che la loro efficacia e sicurezza possano essere confrontate.
Classificazione della ricerca
A una domanda come la classificazione dello studio sui farmaci può essere affrontata da diverse angolazioni. A seconda del fattore, i tipi di studi possono essere diversi. Ecco alcuni metodi di classificazione:
- Secondo il grado di intervento nelle tattiche di gestione del paziente.
- La ricerca può variare nello scopo.
Inoltre, ci sono anche tipi di test di laboratorio. Esaminiamo questa domanda in modo più dettagliato.
Tipi di studi sull'intervento nel trattamento del paziente
Se consideriamo la classificazione in termini di intervento nel trattamento standard, gli studi sono suddivisi in:
- Osservazionale. Nel corso di tale studio, non vi sono interferenze, le informazioni vengono raccolte e il corso naturale di tutti i processi viene monitorato.
- Studio senza intervento o senza intervento. In questo caso, il farmaco è prescritto secondo il solito schema. Nel protocollo di ricerca, la questione della classificazione di un paziente a qualsiasi tattica di trattamento non è decisa in anticipo. La prescrizione del farmaco è chiaramente separata dall'inclusione del paziente nello studio. Il paziente non viene sottoposto ad alcuna procedura diagnostica, i dati vengono analizzati utilizzando metodi epidemiologici.
- Studio interventistico Viene effettuato quando è necessario studiare farmaci non ancora registrati o scoprire nuove direzioni nell'uso di farmaci noti.
Criterio di classificazione - obiettivo di ricerca
A seconda dello scopo, studi clinici generali possono essere:
- Prevenzione. Vengono eseguiti al fine di trovare i modi migliori per prevenire le malattie in una persona che non ha precedentemente sofferto o per prevenire le ricadute. Di solito i vaccini e i preparati vitaminici sono studiati in questo modo.
- Gli studi di screening consentono di trovare il metodo migliore per rilevare le malattie.
- Vengono condotti studi diagnostici per trovare metodi e metodi più efficaci per diagnosticare la malattia.
- Gli studi terapeutici offrono l'opportunità di studiare l'efficacia e la sicurezza dei farmaci, i metodi di terapia.

- Vengono condotti studi sulla qualità della vita per capire come migliorare la qualità della vita dei pazienti con determinate malattie.
- I programmi di accessibilità includono l'uso di un farmaco sperimentale in pazienti con malattie potenzialmente letali. In genere, tali farmaci non possono essere inclusi nei test di laboratorio.
Tipi di ricerca
Oltre ai tipi di studi, ci sono anche tipi che devi conoscere:
- Viene condotto uno studio pilota per raccogliere i dati necessari per le fasi successive dello studio del farmaco.
- Randomizzato comporta la distribuzione casuale dei pazienti in gruppi, hanno l'opportunità di ricevere sia il farmaco in studio che il farmaco di controllo.
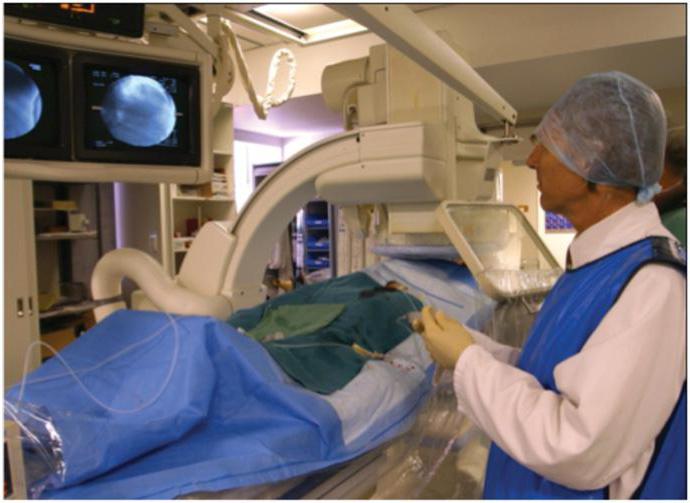
- Uno studio controllato di un farmaco esplora un rimedio sull'efficacia di cui la sicurezza non è ancora nota. Viene confrontato con un farmaco già ben studiato e noto.
- Uno studio non controllato non implica la presenza di un gruppo di controllo di pazienti.
- Uno studio parallelo viene condotto contemporaneamente in diversi gruppi di pazienti che ricevono la medicina studiata.
- Negli studi trasversali, ogni paziente riceve entrambi i farmaci che vengono confrontati.
- Se lo studio è aperto, tutti i partecipanti conoscono il farmaco che il paziente sta assumendo.
- Uno studio cieco o mascherato implica la presenza di due parti che non sono consapevoli della distribuzione dei pazienti in gruppi.
- Viene effettuato uno studio prospettico con la distribuzione dei pazienti in gruppi, che riceveranno o meno il farmaco studiato prima degli esiti.
- In retrospettiva, vengono considerati i risultati degli studi già considerati.
- Un centro di ricerca clinica può essere coinvolto in uno o più, a seconda di ciò, esistono studi a centro singolo o multicentrico.
- In uno studio parallelo, i risultati di diversi gruppi di soggetti vengono confrontati contemporaneamente, tra cui uno è il controllo e due o più altri ricevono il farmaco in studio.
- Uno studio di casi simili comporta il confronto di pazienti con una specifica malattia con quelli che non soffrono di tale malattia al fine di identificare una relazione tra il risultato e la precedente esposizione a determinati fattori.
Fasi di ricerca
Dopo la produzione del farmaco, deve sottoporsi a tutte le ricerche e iniziano con preclinici. Vengono effettuati su animali, aiutano l'azienda farmaceutica a capire se vale la pena esplorare ulteriormente il farmaco.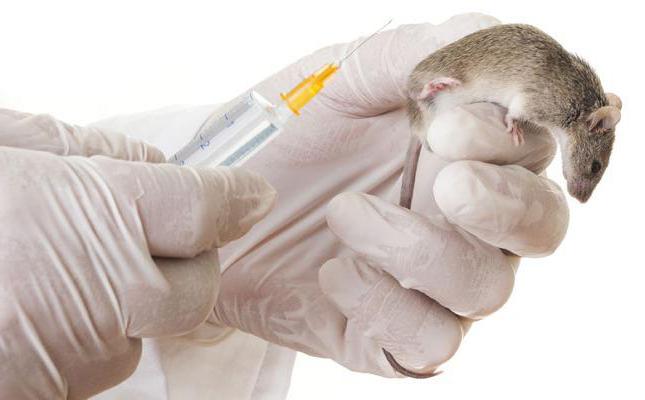
Nell'uomo, inizieranno a testare il medicinale solo dopo aver dimostrato che può essere usato per trattare una determinata condizione e non è pericoloso.
Il processo di sviluppo di qualsiasi farmaco consiste in 4 fasi, ognuna delle quali è uno studio separato. Dopo tre fasi di successo, il farmaco riceve un certificato di registrazione e il quarto è già uno studio post-registrazione.
Fase uno
Una sperimentazione clinica del farmaco nella prima fase si riduce a una serie di volontari da 20 a 100 persone. Se viene esaminato un farmaco troppo tossico, ad esempio per la terapia oncologica, vengono selezionati i pazienti che soffrono di questa malattia.
Molto spesso, la prima fase dello studio viene eseguita in istituzioni speciali, dove c'è personale competente e formato. Durante questa fase, devi scoprire:
- Come viene tollerato il farmaco dall'uomo.
- Proprietà farmacologiche.
- Il periodo di assorbimento ed escrezione dal corpo.
- Pre-valutare la sicurezza della sua ricezione.
Nella prima fase vengono utilizzati vari tipi di ricerca:
- L'uso di dosi crescenti singole del farmaco. Al primo gruppo di soggetti viene iniettata una certa dose del farmaco; se è ben tollerato, il gruppo successivo viene aumentato nel dosaggio. Questo viene fatto fino al raggiungimento dei livelli di sicurezza raggiunti o agli effetti collaterali che iniziano a manifestarsi.
- Studi di dosi incrementali multiple. Un gruppo di volontari riceve ripetutamente un piccolo farmaco, dopo ogni ricevimento, vengono eseguiti i test e viene valutato il comportamento del farmaco nel corpo. Nel gruppo successivo, una dose aumentata viene ripetutamente somministrata, e così via, a un certo livello.
Seconda fase della ricerca
Dopo che la sicurezza del farmaco è stata precedentemente valutata, i metodi di ricerca clinica passano alla fase successiva. Per questo, un gruppo di 50-100 persone sta già reclutando.
L'obiettivo principale in questa fase dello studio del farmaco è determinare il dosaggio e il regime necessari. La quantità di farmaci somministrati ai pazienti in questa fase è leggermente inferiore rispetto alle dosi più elevate ricevute dai soggetti nella prima fase.
In questa fase, c'è sempre un gruppo di controllo. L'efficacia del farmaco viene confrontata con un placebo o un altro farmaco che ha dimostrato di essere altamente efficace nel trattamento di questa malattia.
3 fasi di ricerca
Dopo le prime due fasi, i farmaci continuano ad essere esaminati nella terza fase. Partecipa un folto gruppo di persone fino a 3000 persone. Lo scopo di questo passaggio è confermare l'efficacia e la sicurezza del farmaco.
Anche in questa fase, viene studiata la dipendenza del risultato dal dosaggio del farmaco.
Dopo che il medicinale in questa fase ha confermato la sua sicurezza ed efficacia, viene preparato un fascicolo di registrazione. Contiene informazioni sui risultati dello studio, la composizione del medicinale, la durata di conservazione e le condizioni di conservazione.
Fase 4
Questa fase è già chiamata ricerca post-registrazione.L'obiettivo principale della fase è quello di raccogliere le massime informazioni sui risultati dell'uso prolungato del farmaco da parte di un gran numero di persone.
La questione di come i farmaci interagiscono con altri farmaci, qual è la durata ottimale della terapia, come il farmaco influenza i pazienti di età diverse è ancora allo studio.
Protocollo di studio
Qualsiasi protocollo di ricerca dovrebbe contenere le seguenti informazioni:
- Lo scopo di studiare la medicina.
- I compiti che i ricercatori si sono prefissati.
- Progettazione dello studio
- Metodi di studio
- Domande statistiche
- Organizzazione dello studio stesso.

Lo sviluppo del protocollo inizia anche prima dell'inizio di tutti gli studi. A volte questa procedura può richiedere diversi anni.
Una volta completato lo studio, il protocollo è il documento con cui revisori e ispettori possono verificarlo.
Recentemente, sono stati sempre più ampiamente utilizzati vari metodi di ricerca clinica di laboratorio. Ciò è dovuto al fatto che i principi della medicina basata sull'evidenza vengono attivamente introdotti nell'assistenza sanitaria. Uno di questi è prendere decisioni per la terapia del paziente sulla base di dati scientifici comprovati ed è impossibile ottenerli senza uno studio completo.


